锂离子电池正极材料的现在和未来,拿走不谢!

锂离子电池可以说是目前世界上应用最成熟最广泛的新能源,如手机电脑等便携式电子产品,电动汽车,电动工具,储能项目。特别是当前中国政府和资本疯狂投资支持新能源汽车和动力电池产业的发展,简直到了如火如荼的地步。但是放眼未来,锂电产业还有很长的一段路要走,比如高能量密度体系的开发,成本的进一步降低,资源的回收和利用等问题摆在我们面前。
今天给大家介绍下关于锂离子电池材料的现状和未来发展趋势。
我们知道锂电里所有的材料无非来自于自然界,那首先看一下元素周期表哪些元素能为我们所用呢?
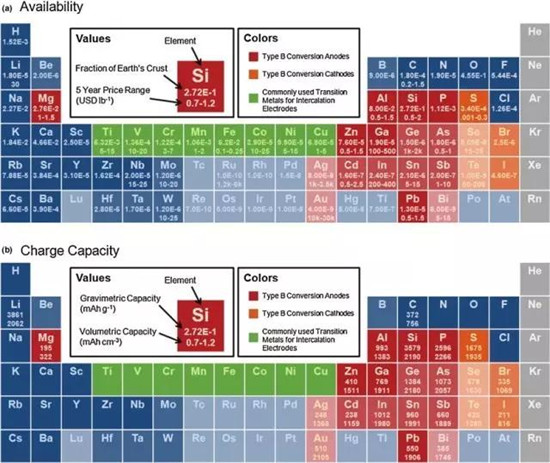
图表a为我们展示了相关各种元素的价格和在地球上的储量,图表b显示了相关元素的质量比容量和体积比容量。
上面只是让大家对正负极材料相关的元素有一个印象,并不能代表化合物本身的性质和可用性,下面大家再看一个更直观和经典的图表。
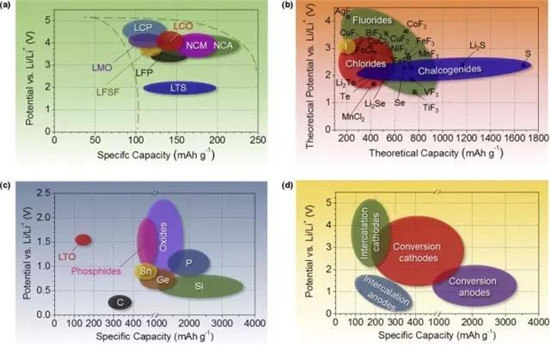
图a是常见的正极材料电位和克容量值(LFSF-氟化铁酸锂铁,LTS-硫化锂钛)
图b是转化型正极材料的电位和克容量值
图c是常见的负极材料电位和克容量值
图d是所有的正负极材料电位和容量的均值
上图可以为研究者对电池电压,容量,电解液,添加剂的选型等提供依据。
新型电池材料的开发方向集中展示在下图,下面将提到一系列代表性的正极和负极材料,从目前商业化可用的材料到可能在未来商业化的有希望的新材料,另外还有一些正负极材料研究的基本性质,机会,挑战和最新进展。
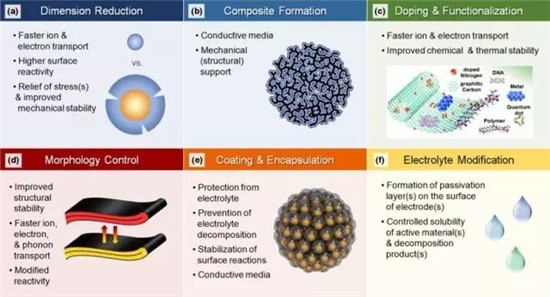
增强电池性能的策略:
a减小活性材料的粒径尺寸:带来更快的离子电子传导率/更高的表面活性/改善机械稳定性
b形成复合材料:引入导电介质/机械支撑机构
c掺杂和接枝官能团
d微调粒子的形态
e表面包覆
f对电解质的改性
正极材料
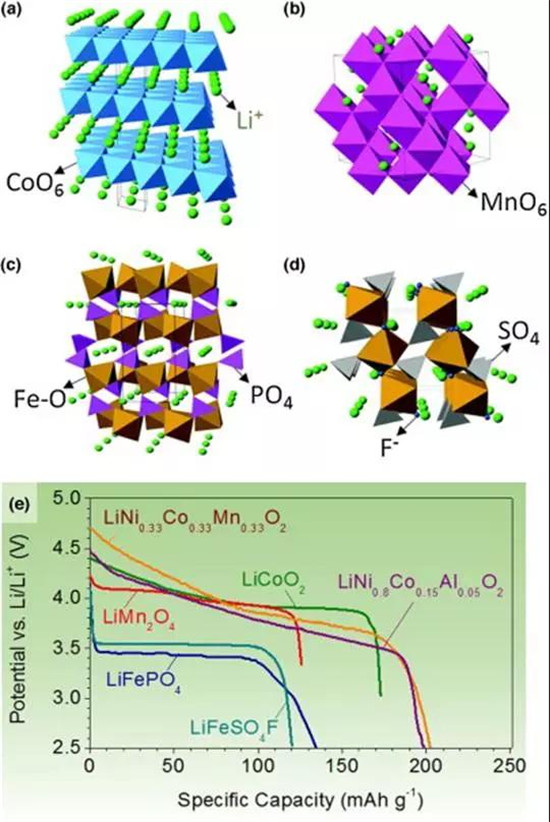
这里主要包括层状LCO,尖晶石LMO,橄榄石LFP等晶体结构。大多数正极材料研究集中在过渡金属氧化物和聚阴离子化合物上,因为它们具有较高的电压和较高的容量(100-200mAh/g和3-5V平均电压)。图e给出了典型的正极材料充放电曲线。
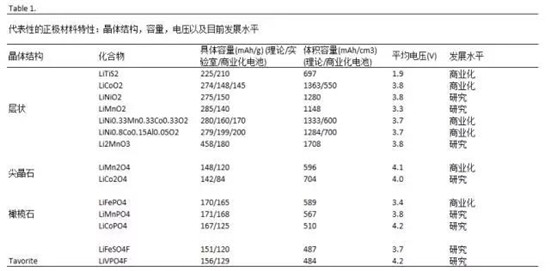
以下列举了具有代表性想正极材料特性以及目前的发展水平
过渡金属氧化物
1.钴酸锂LCO
LCO正极材料是由Goodenough首次提出,并且由Sony首先将其并成功商业化。
优点是高比容量,高电压,低自放电已经良好的循环性能,至今仍广泛应用。
主要的缺点是成本高,热稳定性差和高倍率和深循环的容量的快速衰上。
成本高是由于Co元素的价格高,可以在图一中看到Co的价格。
热稳定性差是指高温150℃状态下正极LCO结构被破坏释放出大量的热造成电池热失控起火爆炸。LCO是目前商业化正极材料中热稳定性最差的。虽然热稳定性也在很大程度上取决于非材料因素,例如电池设计和电池尺寸,但由于释放的氧和有机材料之间的放热反应,LCO通常经历超过200℃的热失控。
深循环(脱锂电位4.2V以上,意味着大约50%以上的Li脱出)导致晶格畸变从而恶化循环性能 。
对LCO的改性方面:对许多不同金属(Mn, Al, Fe, Cr)作为钴掺杂剂/部分代用品进行过研究,虽然证明有一些效果,但对性能的提升有限。各种金属氧化物的涂层(Al2O3, B2O3, TiO2, ZrO2),因为他们的机械和化学稳定性可以减少LCO的结构变化和与电解质的副反应,增强的LCO稳定性,甚至对深循环性能特性有一定改善。
2.镍酸锂LNO
LNO具有和LiCoO相同的晶体结构和275mAh/g的类似理论比容量,与LCO相比主要在成本是低很多,但是LNO的问题在于Ni2+有替代Li+的倾向在脱嵌Li的过程中会堵住Li的扩散通道。安全性和稳定性方面LNO比LCO更容易造成热失控。另外在高SOC条件下的热稳定性差可通过Mg掺杂来改善 ,添加少量Al能提高两者的热稳定性和电化学性能.
3.镍钴铝酸锂NCA
LiNi0.8Co0.15Al0.05O2 (NCA)目前已经被商业化应用,例如松下为Tesla开发的动力电池。其优点在于拥有较高的比容量200mAh/g和相对LCO更好的日历寿命。但在国内刚刚处于起步阶段。关于其失效模式有报道说其在升高的温度下(40-70℃)容量衰减,是由于SEI和微裂纹的生长。
4.锰酸锂LMO
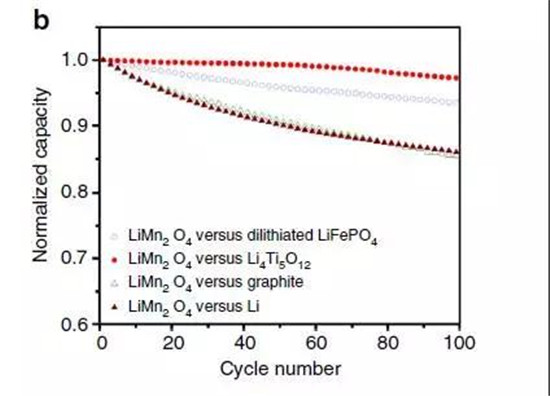
LMO由于其稳定性和较低的成本优势也得到了广泛的应用,但是其主要缺点是较差的循环性能,原因是在Li脱出的过程中其层状结构有变为尖晶石结构的趋势和循环过程中Mn的溶解的不利影响。具体讲是由于Mn3+的歧化反应形成Mn2+和Mn4+,2价Mn离子可以溶解在电解质中破坏负极的SEI,所有含Mn的正极都存在这个反应。伴随着含Mn电极的电池老化,电解质和负极中Mn的含量逐渐增加,石墨负极阻抗变大,这一点已经很明显。但对比LTO负极没有显著的变化(如下图红色曲线)。改性方面一般采用阳离子参杂改善LMO的高温循环稳定性。
5.镍钴锰酸锂NMC
NMC是现今锂离子电池研究的一大热点。与钴酸锂相比,具有以下显著优势:
1.成本低:由于含钴少,成本仅相当于钴酸锂的1/4且更绿色环保。
2.安全性好:安全工作温度可达170℃,而钴酸锂仅为130℃
3.电池的循环使用寿命延长了45%。
另外值得一提的是高Ni三元材料(LiNi 0.8Co 0.1Mn0.1O2)有更高的能量/功率密度(在较高Ni含量下有更多的Li脱出而结构稳定)。而外层是Mn和Co取代的NMC (的LiNi 0.46钴0.23锰0.31 ? 2)为更好的循环寿命和安全性。
聚阴离子化合物
1.磷酸铁锂LFP
LFP拥有良好的热稳定性和功率性能,结构如图4C,其主要缺点是较低的电位和较差的离子导电性。对LFP纳米化,碳包覆和金属参杂是提高其性能的方法。如果不用炭包覆有纳米化的LFP和导电剂均匀混合也同样可实现良好的导电性。然而通常纳米化的LFP电极的低压实密度限制了LFP电池的能量密度。
其它橄榄石结构包括LiMnPO4(LMP),比LFP提高了0.4V的平均电压(表1),从而提高了能量密度。
此外还有Li3V2(PO4)3(LVP)表现出相当高的工作电压(4.0V)和良好的容量(197mAh/ g)。LVP/C纳米复合材料在5C的高速率下表现出95%的理论容量。
2.LiFeSO4F(LFSF)
因为它的高电池电压和合理比容量(151mAh/g) 。而且LiFeSO4F具有更好的离子/电子导电性,因此它不需要碳涂层或纳米化颗粒。
转化正极材料
转化电极在锂化/脱锂期间经历固态氧化还原反应,其中结晶结构发生变化,伴随着断裂和重组的化学键。转化电极材料的完全可逆电化学反应通常如下:
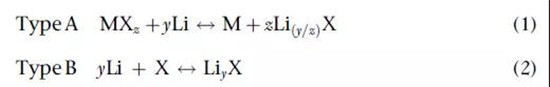
A型的正极中式(1)包括含有高价(2价或更高)的金属离子,可以得到较高的理论容量的金属卤化物。
B型正极包括S, Se, Te, I.其中S因它的高理论比容量(1675mAh/g),成本低,以及在地壳的丰富储量已经被大量研究。
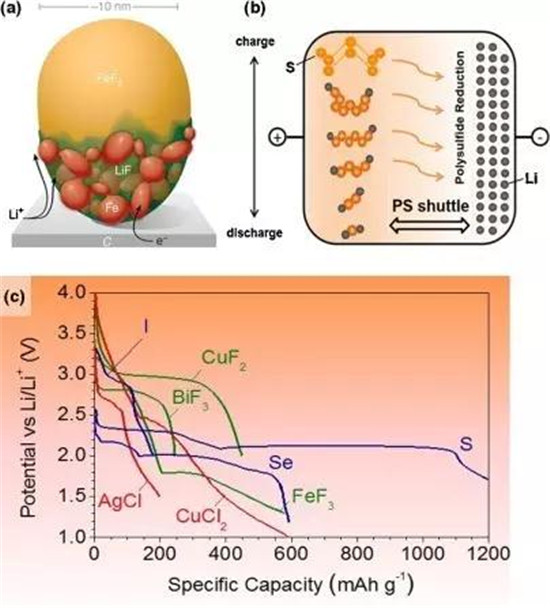
图b显示出了完整的S转化反应,其涉及可溶于有机电解质中间体多硫化物的中间步骤。
图c给出了转换型正极的典型放电曲线。BIF3和CUF2表现出高电压平台。相比较而言,S和Se也显示非常平坦和长电压平台,表示两个固相之间的反应具有良好的动力。
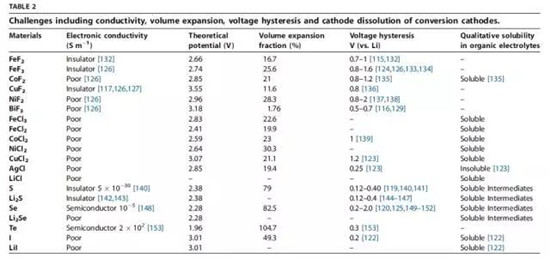
氟和氯化合物
由于中等电压平台和较高的理论比容量,金属氟化物(MF)和氯化物(MCI)近来也已经被积极地研究。然而,MF和MCL通常有比较大的电压滞后,体积膨胀,副反应,和活性材料的溶解(如下图)。大多数MF,包括FEF3和FEF2,是因为金属卤键的高度离子特性引起的带隙大而带来的较差的电子传导性。但他们的开放式结构可以支持良好的离子传导 。相同的原因,氯化物也具有差的电子电导率。
硫和硫化锂
硫具有1675mAh/g的高理论容量,同时还具有成本和丰富的储量优势。然而,缺点是S为主的正极从低电势,低电导率,中间体反应产物(多硫化物)在电解质的溶解,和(在纯S的情况下)非常低汽化温度,其在真空下干燥电极引发S损失。而硫大约80%的体积变化,这可能会破坏碳复合材料在电极的电接触 。
为了减轻溶解和体积膨胀的影响,可以将S包覆在具有过量内部空隙空间的中空结构中。聚乙烯吡咯烷酮聚合物,碳和TiO2 已经通过使用渗透和化学沉淀浸渍硫。当在薄电极构造的半电池中测试时,这些复合材料显示出有时接近1000个循环的循环寿命。
为了避免膨胀,防止干燥过程S蒸发,并形成完整的电池阳极,电极可以制成Li2S的形式。这是因为Li2S具有更高的熔点。
电解液的修饰也是改善S溶解的一个通用方法。LINO3和P2S5添加剂用于形成良好的SEI在Li金属的表面,以防止还原和多硫化物的随后沉淀。也可加入锂多硫化物以暂时降低正极的溶解,固态电解质也可以防止多硫化物的溶解,并在同一时间,通过避免锂枝晶短路增强电池安全。

责任编辑:继电保护
-
权威发布 | 新能源汽车产业顶层设计落地:鼓励“光储充放”,有序推进氢燃料供给体系建设
2020-11-03新能源,汽车,产业,设计 -
中国自主研制的“人造太阳”重力支撑设备正式启运
2020-09-14核聚变,ITER,核电 -
探索 | 既耗能又可供能的数据中心 打造融合型综合能源系统
2020-06-16综合能源服务,新能源消纳,能源互联网
-
新基建助推 数据中心建设将迎爆发期
2020-06-16数据中心,能源互联网,电力新基建 -
泛在电力物联网建设下看电网企业数据变现之路
2019-11-12泛在电力物联网 -
泛在电力物联网建设典型实践案例
2019-10-15泛在电力物联网案例
-
权威发布 | 新能源汽车产业顶层设计落地:鼓励“光储充放”,有序推进氢燃料供给体系建设
2020-11-03新能源,汽车,产业,设计 -
中国自主研制的“人造太阳”重力支撑设备正式启运
2020-09-14核聚变,ITER,核电 -
能源革命和电改政策红利将长期助力储能行业发展
-
探索 | 既耗能又可供能的数据中心 打造融合型综合能源系统
2020-06-16综合能源服务,新能源消纳,能源互联网 -
5G新基建助力智能电网发展
2020-06-125G,智能电网,配电网 -
从智能电网到智能城市